Avec l’IA, les pharmas accélèrent la découverte de nouveaux médicaments

L’IA devrait permettre d’accélérer la découverte de nouvelles molécules pour traiter toute une série de maladies.
Roche
Les géants de l’industrie pharmaceutique, parmi lesquels les groupes suisses Roche et Novartis, misent beaucoup sur l’intelligence artificielle (IA) pour rechercher de nouveaux médicaments destinés à soigner toute une série de maladies. Mais le chemin reste long avant que les traitements découverts par l’IA ne soient mis à la disposition des patients.
La découverte par Matthias Steger du médicament candidat EA-2353 pour le traitement de la rétinite pigmentaire, une maladie oculaire rare et dégénérative, a débuté avec une technologie très rudimentaire: un cahier et un crayon.
Pendant près de dix ans, Matthias Steger, chimiste médicinal de formation, a noté les structures chimiques qui, selon les scientifiques, avaient un impact sur les cellules souches et progénitrices – celles qui peuvent se régénérer dans les tissus endommagés.
Pour parvenir à un médicament candidat, il devait trouver le modèle dans les structures chimiques. Un objectif qui passe par de nombreux tests en laboratoire, nécessitant de longues années et beaucoup d’argent. Et malgré tous ces efforts, des éléments sont laissés au hasard. Avant de devenir entrepreneur, Matthias Steger a passé dix ans dans la recherche de nouveaux médicaments et d’autres fonctions chez Roche.
«Être en quête d’une nouvelle molécule, c’est comme chercher une aiguille dans une botte de foin, indique Matthias Steger. Même pour un chimiste chevronné, il y a une part importante de suppositions.» Il faut en moyenne une décennie et quelque 2,5 milliards de dollars (2,3 milliards de francs suisses) pour mettre un nouveau médicament sur le marché.
Dans l’espoir d’accélérer le processus, il a envoyé les structures chimiques à Gisbert Schneider, un ancien collègue de Roche qui enseigne aujourd’hui la conception de médicaments assistée par ordinateur à l’École polytechnique fédérale de Zurich.
Gisbert Schneider a utilisé ses modèles d’intelligence artificielle pour identifier les molécules ayant l’activité biologique souhaitée en se basant sur les schémas des structures chimiques. Matthias Steger et ses collègues ont testé et synthétisé les molécules durant plusieurs années pour obtenir deux médicaments candidats. L’un d’entre eux, l’EA-2353, fait actuellement l’objet d’essais cliniques précoces.
«Je ne suis pas certain que nous aurions pu trouver le médicament candidat sans l’IA», déclare Matthias Steger, qui a fondé avec Gisbert Schneider la start-up Endogena en 2016. La société, qui compte des bureaux à Zurich et à San Francisco, poursuit le développement des deux médicaments candidats. «Les algorithmes peuvent percevoir des schémas qui ne sont pas visibles à l’œil humain», note le chimiste médicinal.
Le potentiel de l’IA pour découvrir de nouveaux médicaments candidats, avec un gain de temps et d’argent énorme par rapport aux approches traditionnelles, a entraîné un boom de l’investissement dans cette technologie. Selon une étudeLien externe du Boston Consulting Group publiée l’an passé, les investisseurs ont injecté, au cours de la dernière décennie, plus de 18 milliards de dollars dans quelque 200 entreprises de biotechnologie et start-up AI-First. Ces dernières utilisent en priorité l’IA dans leur recherche de nouveaux médicaments.
Contenu externe
Ces sociétés ont été à l’avant-garde de la technologie. Aujourd’hui, à mesure que les médicaments découverts grâce à l’IA sont testés sur des êtres humains, de plus en plus de grandes entreprises pharmaceutiques, dont les géants suisses Roche et Novartis, tentent de prendre de l’avance sur leurs concurrents.
L’an dernier, Roche a annoncé un accord de collaboration pluriannuel dans l’IA avec le fabricant de puces américain Nvidia pour accélérer la découverte de nouveaux médicaments. Depuis 2019, l’entreprise a signé huit accords dans l’IA. En janvier, son concurrent Novartis s’est associé à Isomorphic Labs, spin-off de Google DeepMind qui a reçu un versement initial de 37,5 millions de dollars et pourra percevoir 1,2 milliard de dollars supplémentaires si elle atteint certaines étapes dans le développement de trois nouveaux traitements candidats.
Il ne s’agit là que de quelques exemples parmi la centaine de partenariats conclus entre des entreprises pharmaceutiques et des start-up spécialisées dans la découverte de médicaments par l’IA au cours de la dernière décennie.
Plus
lire plus «Comment ça va, la Suisse?» Participez à notre grand sondage national
Prendre le train en marche
Les grands laboratoires pharmaceutiques utilisent des ordinateurs pour contribuer au développement de médicaments depuis des décennies, mais, jusqu’à récemment, on observait une certaine réticence à s’appuyer trop fortement sur l’IA.
«Après avoir expérimenté les réseaux de neurones artificiels il y a plusieurs années, les entreprises pharmaceutiques ont eu le sentiment, dans les années 2000, que l’IA n’avait pas tenu ses promesses», explique Gisbert Schneider. Ces premiers réseauxLien externe ou algorithmes d’IA manquaient de perfectionnement, de données et de machines puissantes pour effectuer des calculs massifs.
Aujourd’hui, les mentalités ont changé. «Les gens sont nettement plus disposés à accepter les recommandations formulées par un algorithme d’IA, et aucune entreprise pharmaceutique n’entend rester à la traîne.»
L’intelligence artificielle (IA) désigne un ensemble de techniques avancées de calcul et de modélisation qui analysent et apprennent à partir de sources de données souvent vastes et complexes.
Ces techniques peuvent générer des connaissances ou effectuer des tâches à une échelle et à une vitesse qui dépassent les capacités humaines. L’apprentissage profond, qui exploite les réseaux neuronaux artificiels pour acquérir des connaissances à partir de données, est une technologie d’IA couramment utilisée dans la découverte de médicaments.
Source: Boston Consulting Group
Cette évolution s’explique par les récents progrès de l’apprentissage profond, des outils d’IA générative tels que ChatGPT, de la puissance de calcul et des connaissances en génétique et en biologie moléculaire.
La dernière génération de modèles d’IA peut analyser et trouver des modèles dans des ensembles de données vastes et disparates et même dans des images, ce qui la rend extrêmement utile pour la découverte de médicaments lorsque les scientifiques ont affaire à des trillions de cellules et à quelque 20’000 gènes chez une seule personne.
En 2020, DeepMind, la filiale d’IA de Google, a lancé AlphaFold, un algorithme capable de prédire les structures tridimensionnelles des protéines humaines, de l’ARN et de l’ADN. Cet algorithme a permis de déterminer la structure d’une protéine clé du SARS-CoV-2, aidant ainsi les scientifiques à mettre au point des vaccins contre le Covid-19 en un temps record.
AlphaFold a non seulement alimenté la recherche sur une série de nouvelles cibles médicamenteuses, mais a également confirmé le potentiel de l’IA en matière de percées scientifiques.
Il existe aujourd’hui une multitude d’outils logiciels d’IA propriétaires et libres, déployés dans les entreprises pharmaceutiques pour rechercher des données pertinentes à travers les revues médicales, passer au crible les bibliothèques de molécules à la recherche de médicaments candidats prometteurs et identifier les pathologies cibles. D’après certaines étudesLien externe, l’IA pourrait réduire de 25 à 50% le temps et le coût de la découverte de médicaments.
Plus
lire plus Des vaccins en un temps record grâce à l’intelligence artificielle
«L’IA, y compris l’apprentissage automatique et les grands modèles de langage, n’est pas une technologie entièrement nouvelle, relève Elif Ozkirimli, à la tête du secteur des produits informatiques pour la recherche et le développement (R&D) chez Roche à Bâle. Mais l’adoption de l’IA et son échelle se sont considérablement accélérées au cours des deux dernières années.»
Roche a investi quelque trois milliards de dollars par an pour moderniser son infrastructure numérique et intégrer davantage l’IA dans ses processus de R&D, selon une récente présentation aux investisseursLien externe.
Il y a quelques années, le laboratoire a engagé des bio-informaticiens de haut niveau du Massachusetts Institute of Technology (MIT) et de l’Université de Cambridge pour constituer une équipe de pas moins de 400 personnes au sein du département des sciences informatiques de sa filiale Genentech de San Francisco. Des centaines d’autres personnes travaillent à Bâle et sur d’autres sites.
En 2021, Roche a racheté Prescient Design, une start-up new-yorkaise de trois personnes, pour créer une série d’algorithmes formés à partir de données publiques et de données propres à l’entreprise, issues d’expériences et d’essais cliniques. Ces algorithmes ont déjà été utilisés pour trouver de nouvelles indications sur des médicaments plus anciens et classer par ordre de priorité les traitements candidats dans le pipeline ayant les meilleures chances de succès.
De la recherche à la création
En plus de rendre la découverte de médicaments plus efficace, l’IA a le potentiel d’identifier et même de générer des molécules dont les chimistes n’avaient même pas rêvé. Certains algorithmes, comme celui que Gisbert Schneider a utilisé pour Endogena, créent même des molécules à partir de zéro.
«Au lieu de chercher des médicaments en passant les molécules au crible les unes après les autres, l’IA générative inverse le processus. Elle nous permet de concevoir des molécules dotées de certaines propriétés au lieu de les rechercher», souligne Gisbert Schneider.
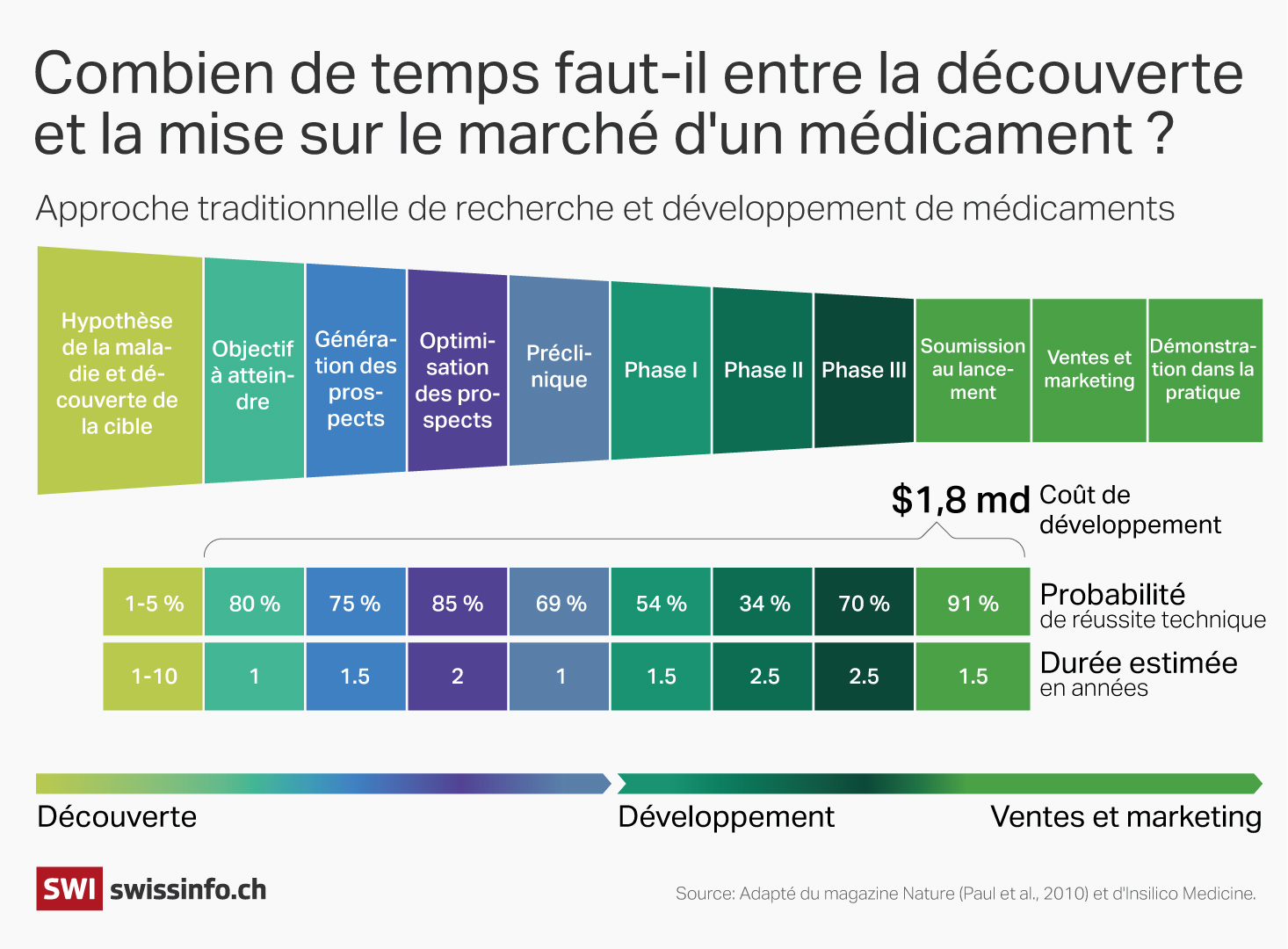
Kai Reusser / SWI swissinfo.ch
Plusieurs jeunes entreprises s’y emploient déjà. Insilico Medicine, une start-up basée à Hong Kong, a utilisé des modèles d’IA pour identifier une cible thérapeutique (molécule associée à une maladie) et créer une structure moléculaire semblable à celle d’un médicament contre la fibrose pulmonaire, une grave maladie des poumons.
Le traitement candidat, qui fait actuellement l’objet d’essais de phase II, a été découvert en dix-huit mois et pour un coût de 3 millions de dollars, soit beaucoup moins qu’avec des approches traditionnelles. En 2022, le géant pharmaceutique français Sanofi a signé un partenariat de 1,2 milliard de dollars avec Insilico Medicine pour identifier des cibles thérapeutiques et faire progresser les médicaments candidats.
Les chimistes et les informaticiens de Genentech ont mis au point un cadre d’apprentissage profond appelé GNEProp pour identifier de petites molécules antibiotiques efficaces contre les «superbactéries», des bactéries qui résistent aux antibiotiques. Certaines des molécules produites par l’algorithme possèdent des structures complètement différentes de celles utilisées pour constituer le modèle.
L’entreprise teste certaines de ces molécules en phase préclinique avant de les insérer dans des modèles d’IA sur la base des résultats obtenus en laboratoire. L’objectif est d’établir des prédictions plus précises à l’avenir.
«La découverte de médicaments est une approche par essais et par erreurs, selon Elif Ozkirimli. Avec l’IA, nous essayons d’intégrer certains de ces essais et erreurs dans les modèles d’apprentissage automatique pour qu’ils puissent réaliser de meilleures prédictions.»
Un marathon plutôt qu’un sprint
Malgré les investissements massifs et l’enthousiasme suscité par les nouvelles découvertes, les entreprises pharmaceutiques demeurent prudentes lorsqu’il s’agit de vanter les mérites de l’IA. Ni Roche ni Novartis ne communiquent les noms des médicaments découverts par l’IA faisant l’objet d’essais cliniques. La découverte à partir d’un écran d’ordinateur ou même d’un laboratoire ne permet pas toujours de prédire le succès chez les patients.
Le développement de médicaments connaît un taux d’échec élevé: environ neuf médicaments sur dix découverts par des méthodes traditionnelles échouent lors des essais cliniques, lorsque la sécurité et l’efficacité des traitements sont testées chez l’être humain. Il est trop tôt pour dire si les médicaments conçus par l’IA auront plus de chance et pour déterminer les algorithmes d’IA permettant des prédictions plus précises.
Plus
lire plus La Suisse, pays des géants pharmaceutiques, veut attirer les start-up de l’IA
«Nous ignorons encore beaucoup de choses sur la biologie humaine, l’évolution des maladies et les raisons pour lesquelles certains patients réagissent mieux aux médicaments que d’autres, fait remarquer Gisbert Schneider. On a tendance aujourd’hui à exagérer les avantages potentiels des outils d’IA, car nous oublions la part de chaos lorsque nous interagissons avec la biologie humaine.»
Selon une étudeLien externe publiée en avril, au moins 75 médicaments candidats ayant fait l’objet d’essais cliniques au cours de la dernière décennie ont été mis au point par des entreprises «AI-First». Quelque 80 à 90% des candidats qui ont passé la phase 1 des essais cliniques ont été couronnés de succès. Ce chiffre est supérieur à la moyenne de l’industrie, qui atteint 50 à 60%.
Toutefois, des expertsLien externe ont critiqué la méthodologie de l’étude, arguant que le degré d’utilisation de l’IA pour la conception de ces médicaments variait considérablement, ce qui rendait difficile toute généralisation quant au succès de l’IA. En outre, la phase 2, au cours de laquelle les médicaments sont testés sur un nombre de patients nettement plus important, est considérée comme un facteur plus déterminant pour la mise sur le marché d’un médicament.
Certains traitements candidats ont déjà essuyé des revers. En octobre dernier, une start-up, Exscientia, a dit mettre fin à un essai clinique précoce de son médicament candidat contre le cancer basé sur l’IA, l’EXS-21546. Cette annonce est survenue quelques mois après qu’un autre produit de la société londonienne BenevolentAI conçu à partir de l’IA s’est montré moins efficace qu’espéré lors des premiers essais.
«La plupart des médicaments échouent non pas parce que la molécule est défectueuse. Dans de nombreux cas, la molécule fait exactement ce qu’elle devrait faire, pointe Matthias Steger. Le lien entre la biologie moléculaire et la pathologie du patient n’est tout simplement pas aussi évident que le prévoyait l’hypothèse.»
Texte relu et vérifié par Virginie Mangin/ds, traduit de l’anglais par Zélie Schaller/dbu

